COI の開示
演題発表内容に関連し、発表者らに開示すべきCOI関係にある企業などはありません。
本日の議題について
今日のテーマは次の通りです。
- ライソゾーム病(LSD)の酵素活性測定法について
- Population-based screening について
日本でやる場合、どうすべきかというテーマをいただいていますので、後半以降に、台湾やアメリカの状況を紹介しながら、日本にどのように還元すべきかをお話ししたいと思います。
- 好適なスクリーニング法について
それから、かなり悩んだのですが、好適なスクリーニング法が1 つなのかというのはいろいろ議論のあるところです。いろいろな方法があるかと思いますけれども、例えば、MS/MSを利用する場合にも、Flow-injection 法がいいか、LC-MS/MS法がいいかも議論になるところです。それから、例えば、前処理を溶媒抽出にするか、固相抽出にするか、カラムスイッチング法にするか、もしくは何もせずに直接打ち込むか、これも重要な問題になるかと思います。
LC-MS/MS法の時も、分析カラムをどうするかとか、溶媒のメタノールをどうするか、アセトニトリルにするか、そういうところも、議論すれば幅が出てくるわけです。結局は何が大事なのかを考えました。
1 つの集約的な議論として、遺伝子検査の実施の数を減らすにはどうしたらいいのかというところにたどり着けないか。それも実際的には重要な問題なのではないかということでお話をしたいと思います。
私の専門は脂質生化学で、現在は臨床検査学、バイオマーカー、ライソゾーム病を専門にしています。所属学会は、質量分析学会、脂質生化学会、日本マススクリーニング学会、日本先天代謝異常学会などです。日本医用マススペクトル学会では、昨年から評議員になりました。
もう1 つ、私は「クロマトグラファー」ではあって、「マス(質量分析)屋」ではありません。質量分析はテクニックとして非常に有用ですが、私の専門は脂質生化学なので、クロマトグラファーです。
LC-MS/MS法の時も、分析カラムをどうするかとか、溶媒のメタノールをどうするか、アセトニトリルにするか、そういうところも、議論すれば幅が出てくるわけです。結局は何が大事なのかを考えました。
1 つの集約的な議論として、遺伝子検査の実施の数を減らすにはどうしたらいいのかというところにたどり着けないか。それも実際的には重要な問題なのではないかということでお話をしたいと思います。
私の専門は脂質生化学で、現在は臨床検査学、バイオマーカー、ライソゾーム病を専門にしています。所属学会は、質量分析学会、脂質生化学会、日本マススクリーニング学会、日本先天代謝異常学会などです。日本医用マススペクトル学会では、昨年から評議員になりました。
もう1 つ、私は「クロマトグラファー」ではあって、「マス(質量分析)屋」ではありません。質量分析はテクニックとして非常に有用ですが、私の専門は脂質生化学なので、クロマトグラファーです。
ライソゾーム病について
ライソゾーム病について簡単に説明します。
- ライソゾーム病は遺伝性小児疾患で、約60 遺伝子、100 病態位が知られています。
- 脂質、糖脂質、糖、ムコ多糖、その他の生化学物質(バイオマーカー)が蓄積するのが1 つの大きな特徴です。
- オートファジーとの関連も指摘されています。
オートファジーは2016 年、大隅良典先生がノーベル賞を受賞されたことで一躍有名になりました。ライソゾームの歴史ということでは、ベルギーご出身のChristian de Duve 先生が、今から40年ぐらい前にライソゾームやペルオキシソームを発見した業績でノーベル生理学・医学賞を受賞されています。
- ライソゾーム病は十数疾患で治療法が開発されています。
- 分析技術の高感度化に伴う早期診断が可能になってきています。
ライソゾーム病の検査方法の発達
ライソゾーム病の検査の方法論です。アルゼンチン出身のNestor A Chamoles先生が、2001年にDBS(乾燥ろ紙血)でライソゾーム病の酵素が安定であることを示しました。これは非常に簡単な実験でしたが、この事実はすごく重要で、これによって、今DBSをパンチして酵素活性を測定することが可能になっています。残念なことに、Nestor A Chamoles先生は2007年に60歳の若さで亡くなられたとつい最近伺いました。
この3年後の2004年、ワシントン大学のMichael Gelb 先生がMS/MS法の第一報を発表しました。
2011年には、デューク大学のDavid S Millington先生が中心になって開発した液滴微小流路系(digital microfluidics)という方法が論文報告されてます。
この3年後の2004年、ワシントン大学のMichael Gelb 先生がMS/MS法の第一報を発表しました。
2011年には、デューク大学のDavid S Millington先生が中心になって開発した液滴微小流路系(digital microfluidics)という方法が論文報告されてます。
ライソゾーム病の酵素活性の測定方法
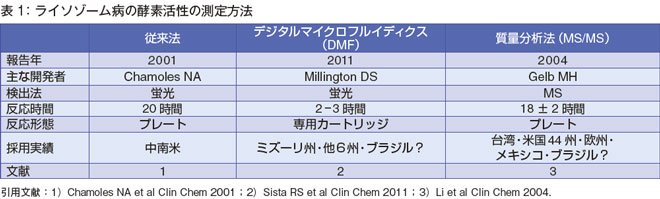
酵素活性の測定方法には、従来法(蛍光法)、digital microfluidics(DMF)、質量分析法(MS/MS)の3つがあります。digital microfluidics の検出法は、蛍光を使用しています。
3つの方法のうち、従来法は蛍光法で、20時間ぐらいインキュベーションします。
Digital microfluidics 法は、専用カートリッジで、インキュベーション時間は短く、検出は蛍光です。質量分析法(MS/MS)は、20時間くらいインキュベーションします。
採用の実績ですが、従来法は中南米で割と多いです。digital microfluidics は、ミズーリ州を含めて6 州位と聞いています(検査会社ホームページからの情報)。質量分析法(MS/MS)を採用しているところが結構多く、台湾、米国などです。ヨーロッパはオーストリア、ハンガリーで、イタリアではパイロットで採用しています。メキシコでは、5 万検体位でパイロットを実施したという論文報告が2011 年にありました。ブラジルでは、digital microfluidics で実施するか、MS/MSにするか、両方パイロットを実施して悩んでいるそうです。たまたま学会でブラジルの先生と隣になったことがあって、聞いたのですが、「ALDはどうするんですか?」と質問したら、「そうなんだよね」と言っていました。皆さん悩んでいるようです。
3つの方法のうち、従来法は蛍光法で、20時間ぐらいインキュベーションします。
Digital microfluidics 法は、専用カートリッジで、インキュベーション時間は短く、検出は蛍光です。質量分析法(MS/MS)は、20時間くらいインキュベーションします。
採用の実績ですが、従来法は中南米で割と多いです。digital microfluidics は、ミズーリ州を含めて6 州位と聞いています(検査会社ホームページからの情報)。質量分析法(MS/MS)を採用しているところが結構多く、台湾、米国などです。ヨーロッパはオーストリア、ハンガリーで、イタリアではパイロットで採用しています。メキシコでは、5 万検体位でパイロットを実施したという論文報告が2011 年にありました。ブラジルでは、digital microfluidics で実施するか、MS/MSにするか、両方パイロットを実施して悩んでいるそうです。たまたま学会でブラジルの先生と隣になったことがあって、聞いたのですが、「ALDはどうするんですか?」と質問したら、「そうなんだよね」と言っていました。皆さん悩んでいるようです。
従来法(蛍光法、Nestor A Chamoles らの原法)
従来法(蛍光法)は2001年、Nestor A Chamoles先生が、2001年の論文“Diagnosis of α-L- Iduronidase Deficiency in Dried Blood Spots on Filter Paper: The Possibility of Newborn Diagnosis”で発表されています。非常に簡単な実験方法で、20時間のインキュベーションでDBSを使うと酵素反応生成物が上がり、罹患者では上がりません。DBS中では酵素活性が安定である事実を示しています。
基質は、当時、newborn screeningが頭の中にあったかどうかわかりませんが、手近にある蛍光基質を使用しています。それが現在も続いています。これが歴史的な話です。
基質は、当時、newborn screeningが頭の中にあったかどうかわかりませんが、手近にある蛍光基質を使用しています。それが現在も続いています。これが歴史的な話です。
Digital microfluidics(DMF)(液滴微小流路)技術を用いた方法
Digital microfluidics は、日本語では液滴微小流路系という日本語訳になると思います。
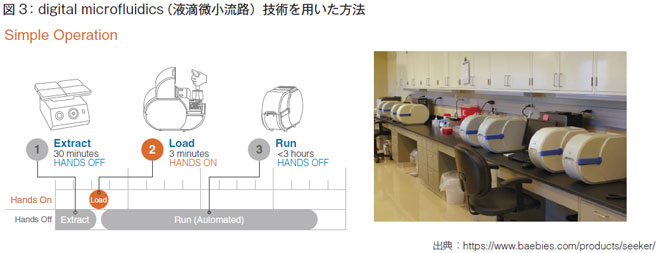
図3 はBaebies 社のホームページにある、ミズーリ州のラボの様子です。酵素をシェーカーで30 分撹拌・抽出して、マルチチャンネルで検体を入れ、それを3時間反応させると、最終的に生成物ができるので、それを蛍光で検出するという方法です。
図3 はBaebies 社のホームページにある、ミズーリ州のラボの様子です。酵素をシェーカーで30 分撹拌・抽出して、マルチチャンネルで検体を入れ、それを3時間反応させると、最終的に生成物ができるので、それを蛍光で検出するという方法です。
タンデム質量分析法(MS/MS)を利用した酵素活性測定法
タンデム質量分析法はワシントン大学のMichael Gelb 先生が考案されました。
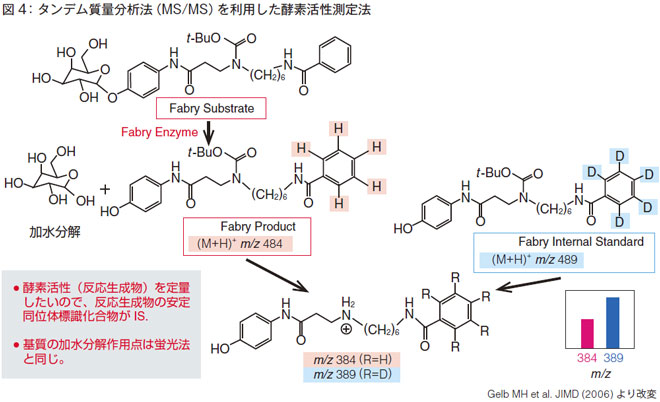
この方法について、ファブリー病の場合を例にして説明します。図4にある基質Fabry Substrate がまず、DBS中の酵素と反応します。すると、一定時間の反応後、加水分解されてFabry Product が生成されます。このProduct と同じ構造で、青いところが重水素でラベルされた標準物質Fabry Internal Standard が、あらかじめ基質と一緒に混ざっていいます。これを一緒に分析すると、イオンサプレッションがあったとしても、標準物質Fabry Internal Standard のイオン強度とFabry Product の強度が同じに変動して、酵素活性の定量範囲をより広く測定することができます。これがタンデム質量分析法の特徴です。
繰り返しになりますけれども、最初に基質Substrate と反応するので、バックグラウンドとしてProduct はほとんどないことが基質の調整法として非常に重要だそうです。低バックグラウンドのところでm/z値が出てくるので、赤(検体)と青(標準)を比較することで測定できるのというが基本原理です。
この方法について、ファブリー病の場合を例にして説明します。図4にある基質Fabry Substrate がまず、DBS中の酵素と反応します。すると、一定時間の反応後、加水分解されてFabry Product が生成されます。このProduct と同じ構造で、青いところが重水素でラベルされた標準物質Fabry Internal Standard が、あらかじめ基質と一緒に混ざっていいます。これを一緒に分析すると、イオンサプレッションがあったとしても、標準物質Fabry Internal Standard のイオン強度とFabry Product の強度が同じに変動して、酵素活性の定量範囲をより広く測定することができます。これがタンデム質量分析法の特徴です。
繰り返しになりますけれども、最初に基質Substrate と反応するので、バックグラウンドとしてProduct はほとんどないことが基質の調整法として非常に重要だそうです。低バックグラウンドのところでm/z値が出てくるので、赤(検体)と青(標準)を比較することで測定できるのというが基本原理です。
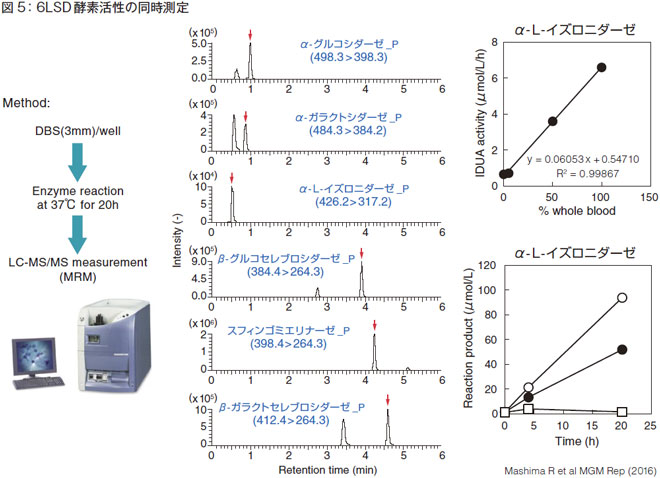
実際にライソゾーム病6 疾患の酵素活性を測定した3 年ほど前の経験をお話します。方法としては、まずDBSにEnzymeを反応させてProduct を生成し、それをLC-MS/MSで測定します。
上から2 番目のα-ガラクトシダーゼ(GLA-P)の場合、目的物(矢印あり)と違うピークがすぐ左近くにあります。もしこれをFlow-injection でやると、一緒に足し算されることになり、バックグラウンドが最初から高値になります。私はクロマトグラファーだったので、本能的に、こういうのはクロマトをかけた方がよいと思い分離したのですが、実はそれが重要だと後から知りました。
100%血液、50%血液、0%血液で実験しても定量性は得られますし、経時的に酵素反応生成物を追跡した実験でも大体直線的な関係が得られました。
上から2 番目のα-ガラクトシダーゼ(GLA-P)の場合、目的物(矢印あり)と違うピークがすぐ左近くにあります。もしこれをFlow-injection でやると、一緒に足し算されることになり、バックグラウンドが最初から高値になります。私はクロマトグラファーだったので、本能的に、こういうのはクロマトをかけた方がよいと思い分離したのですが、実はそれが重要だと後から知りました。
100%血液、50%血液、0%血液で実験しても定量性は得られますし、経時的に酵素反応生成物を追跡した実験でも大体直線的な関係が得られました。
採用例その1(台湾):遺伝的背景が比較的均一で、特定の変異が多い場合
それでは、ライソゾーム病の測定例についての報告を幾つか紹介していきたいと思います。
まず、台湾のMS/MSの最初の例です。台湾は遺伝的な背景が比較的均一で、特定の変異が多いとされています。
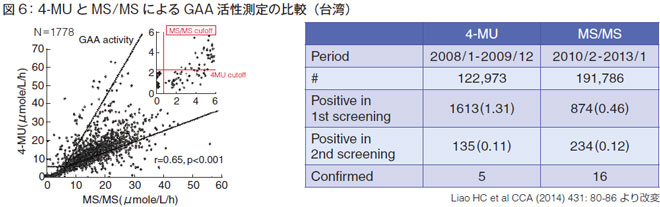
GAA活性をDBSを使ってMS/MSと4MUで測定比較しました(図6)。データは横軸はMS/MS、縦軸は4MUです。基本的に幾らかばらけるのですけれども、重要なのは、原点付近のところです。データにカットオフラインを入れてみました。すると、4MUのラインの右下あたりに点がたくさんあって、そこがフォールス・ポジティブになります。MS/MSでは、縦軸の0~1の付近には点がありますが、上の方の2~6の領域にはありません。
1st screening のポジティブ数は、4MU は1.31 %、MS/MS は0.46 % で、手間は3 分の1 になるわけです。2ndscreening での罹患頻度はほぼ同じなので、1stの手間が少ないMS/MS法を、台湾では使用しています。
まず、台湾のMS/MSの最初の例です。台湾は遺伝的な背景が比較的均一で、特定の変異が多いとされています。
GAA活性をDBSを使ってMS/MSと4MUで測定比較しました(図6)。データは横軸はMS/MS、縦軸は4MUです。基本的に幾らかばらけるのですけれども、重要なのは、原点付近のところです。データにカットオフラインを入れてみました。すると、4MUのラインの右下あたりに点がたくさんあって、そこがフォールス・ポジティブになります。MS/MSでは、縦軸の0~1の付近には点がありますが、上の方の2~6の領域にはありません。
1st screening のポジティブ数は、4MU は1.31 %、MS/MS は0.46 % で、手間は3 分の1 になるわけです。2ndscreening での罹患頻度はほぼ同じなので、1stの手間が少ないMS/MS法を、台湾では使用しています。
台湾に多い遅発型ファブリー病に対する対応
実は、台湾ではもう1つ問題があります。ファブリー病の遅発型病的変異IVS4+919G>A(スプライシングバリアント)が台湾人に多いことが判明しています。
その発現頻度は男子1/1,471、女子1/3,756です。遅発型は、新生児のときにスクリーニングしても病気は発症しません。では、いつから発症するかというと、30~39歳からだんだん右肩上がりになっていって、70~79歳で100%になります。ファブリー病の新生児スクリーニングをやって、すぐに酵素補充療法を開始したという話もありましたが、現在は治療のガイドラインが変わって、40歳になったら病院に来てくださいと伝えるそうです。治療のオプションもいろいろあり、費用対効果がうまくいくようにしているというのが今の台湾です。
その発現頻度は男子1/1,471、女子1/3,756です。遅発型は、新生児のときにスクリーニングしても病気は発症しません。では、いつから発症するかというと、30~39歳からだんだん右肩上がりになっていって、70~79歳で100%になります。ファブリー病の新生児スクリーニングをやって、すぐに酵素補充療法を開始したという話もありましたが、現在は治療のガイドラインが変わって、40歳になったら病院に来てくださいと伝えるそうです。治療のオプションもいろいろあり、費用対効果がうまくいくようにしているというのが今の台湾です。
日本人のポンペ病の新生児スクリーニングデータとG576S
日本でもライソゾーム病の遺伝子変異の割合や特徴的な変異について調査しています。そういう研究は、別にMS/MSでやる必要はなく、4MUの時代のデータが厳然と生きています。
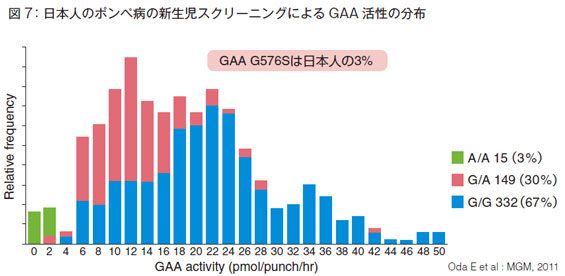
図7は2011年に報告された日本人におけるポンぺ病の新生児スクリーニングのデータです。緑色のところはポンぺ病の機能多型G576Sの分布で、日本人で3%いることがわかっています。機能多型なので遺伝子に変異があり、酵素活性も低いのですが、追跡調査してもこの集団は病気にはなりません。G576Sの人たちは正常と判断されて取り扱われることが望ましいのですが、低活性なので悩ましいわけです。
例えば、東京都の10万人位を分母にすると、罹患者は10万分の1位と言われているので、1人/ 年位の頻度ですが、機能多型は3%なので、3000人/ 年という計算になります。実際に測定すると、大変なことになるわけです。日本全体で新生児スクリーニングを開始する前に、こうした問題を今の段階で議論し解決しておく必要があると思います。
図7は2011年に報告された日本人におけるポンぺ病の新生児スクリーニングのデータです。緑色のところはポンぺ病の機能多型G576Sの分布で、日本人で3%いることがわかっています。機能多型なので遺伝子に変異があり、酵素活性も低いのですが、追跡調査してもこの集団は病気にはなりません。G576Sの人たちは正常と判断されて取り扱われることが望ましいのですが、低活性なので悩ましいわけです。
例えば、東京都の10万人位を分母にすると、罹患者は10万分の1位と言われているので、1人/ 年位の頻度ですが、機能多型は3%なので、3000人/ 年という計算になります。実際に測定すると、大変なことになるわけです。日本全体で新生児スクリーニングを開始する前に、こうした問題を今の段階で議論し解決しておく必要があると思います。
ポンぺ病における乳児型ポンぺ病(infantile-onset Pompe disease,IOPD)と機能多型(GAAG576S)の区別について
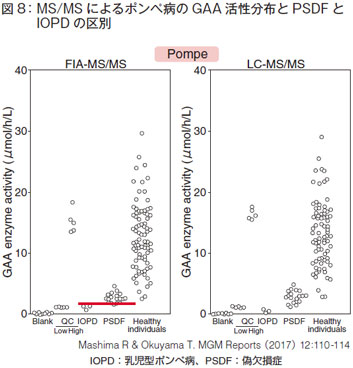 遺伝子変異のうち、ある特定の変異で罹患することがわかっているものは病的変異、ある特定の変異で罹患しないことがわかっている遺伝的変異は機能多型です。偽欠損症は酵素は低活性ですが全部同じ遺伝子型を持っていて罹患しない集団です。
遺伝子変異のうち、ある特定の変異で罹患することがわかっているものは病的変異、ある特定の変異で罹患しないことがわかっている遺伝的変異は機能多型です。偽欠損症は酵素は低活性ですが全部同じ遺伝子型を持っていて罹患しない集団です。ポンぺ病の場合、G576Sによる機能多型の変異が偽欠損症と判断されますが、それをMS/MSで測定したデータが図8です。赤線を引くと、乳児型ポンぺ病(infantile-onset Pompe disease, IOPD)と偽欠損症(pseudodeficiency, PSDF)は、下と上できっちり分かれています。
厳密でなくても、次のステップの検査の手間を考えると、なるべく分けて測定できる方法がいいと思います。そうしたときにFlow-injectionの方がいいか、LC-MS/MSの方がいいかをみてみます。LC-MS/MSのほうが精度がよいですが、Flow-injection でもそこそこいけることがわかります。1st screeningはFlow-injectionでガーッとかけて、その後、低活性ものだけLC-MS/MSで測定するというのも、否定されるものではないと思います。
日本人に多いムコ多糖症Ⅱ型の多型(T500I など)
ムコ多糖Ⅱ型の遺伝子の型、エクソンを見ると、9個あることがわかっています。我々が報告したのですが、病的変異にも2種類あって、脳に障害が出るもの、出ないものがあります。出ないものの多くは一塩基置換やアミノ酸の変異が多く、出るものはリコンビネーションとか比較的大きくたんぱく質の部分がなくなるものが多いです。
ポンぺ病と同様に、病的変異があれば多型もあります。台湾の研究では、今日、御出席の吉田先生が先天代謝異常学会で報告されたT500Iの変異やP284Lもあります。
また、一番のエクソンと2 番のエクソンの間のイントロンには22の塩基がありますが、トランスクリプトは同じですが発現レベルが下がり、酵素活性が低下する多型があることが知られています。最終的に病気にならず、正常と取り扱われてよく、報告例もあまりありません。多型であれ、病的変異であれ、スクリーニングをかける集団にどういう変異があるかを把握している必要があると思います。
ポンぺ病と同様に、病的変異があれば多型もあります。台湾の研究では、今日、御出席の吉田先生が先天代謝異常学会で報告されたT500Iの変異やP284Lもあります。
また、一番のエクソンと2 番のエクソンの間のイントロンには22の塩基がありますが、トランスクリプトは同じですが発現レベルが下がり、酵素活性が低下する多型があることが知られています。最終的に病気にならず、正常と取り扱われてよく、報告例もあまりありません。多型であれ、病的変異であれ、スクリーニングをかける集団にどういう変異があるかを把握している必要があると思います。
ID2S の酵素活性測定法の経緯からわかる重要点
MPSⅡのID2Sの酵素活性の測定結果について少しお話します。
2013 年にワシントン大学のGelb 研究室で、MPSⅡのID2Sの酵素活性をMS/MSで最初に測定したデータが報告されました。6plexと3plexのID2Sがあって、これらを溶液の状態で混ぜて9plexとして測定したときの酵素活性は0.10で、分けて測定した時の酵素活性は0.60で、分けて測定した酵素活性が高いことがわかりました。
その後、基質を変えたり、pHを変え、反応条件を変えたりすると、酵素活性の平均値が高くなったり、我々の報告でも分布は大きく変わっています。
先ほどの多型の話にもありましたが、罹患者とControls のところの空間は非常に重要で、Controls の酵素活性がゼロに迫ると区別しにくくなります。最初の段階のところで、Controls と多型と罹患者の酵素活性の区別が、ある程度あいた状態になっていることは重要です。
そのためには、例えば、どの酵素を選ぶかということも重要です。ライソゾーム病ではどの酵素をはかるかという議論があります。
pHも重要でしょう。塩濃度、界面活性剤の種類とか濃度とかも全部重要です。ライソゾームの酵素と言いますが、全部の条件が同時にそろうわけではありません。盲目的に混ぜた例はありますけど、混ぜればいいというものではなく、結果の確認はある程度重要です。先行研究もある程度ありますから、それを踏襲した形のほうが、比較的無難ではないかと思います。
2013 年にワシントン大学のGelb 研究室で、MPSⅡのID2Sの酵素活性をMS/MSで最初に測定したデータが報告されました。6plexと3plexのID2Sがあって、これらを溶液の状態で混ぜて9plexとして測定したときの酵素活性は0.10で、分けて測定した時の酵素活性は0.60で、分けて測定した酵素活性が高いことがわかりました。
その後、基質を変えたり、pHを変え、反応条件を変えたりすると、酵素活性の平均値が高くなったり、我々の報告でも分布は大きく変わっています。
先ほどの多型の話にもありましたが、罹患者とControls のところの空間は非常に重要で、Controls の酵素活性がゼロに迫ると区別しにくくなります。最初の段階のところで、Controls と多型と罹患者の酵素活性の区別が、ある程度あいた状態になっていることは重要です。
そのためには、例えば、どの酵素を選ぶかということも重要です。ライソゾーム病ではどの酵素をはかるかという議論があります。
pHも重要でしょう。塩濃度、界面活性剤の種類とか濃度とかも全部重要です。ライソゾームの酵素と言いますが、全部の条件が同時にそろうわけではありません。盲目的に混ぜた例はありますけど、混ぜればいいというものではなく、結果の確認はある程度重要です。先行研究もある程度ありますから、それを踏襲した形のほうが、比較的無難ではないかと思います。
Population-based screening における方法論選択の考え方
 Population-based screening を日本で行う場合の方法論選択の考え方についてお話します。
Population-based screening を日本で行う場合の方法論選択の考え方についてお話します。日本人には固有の多型、病的変異がまずあります。これが重要です。その他に、東京などの大都市ではあるかもしれない水平伝搬として持ち込まれるものがあるでしょう。さらに、コンパウンドヘテロでさらに追加の変異が入って罹患となるものや遺伝的に進化する形もあると思います。そういうものが検討の対象にはなると思います。
スクリーニングをする場合、固有の多型や病的変異をどの位正確に区別できるかがポイントになります。効率よくスクリーニングをかけるような型の構築が重要です。
米国ニューヨークのような遺伝的背景が複雑な極端な例のお話をします。ニューヨーク州に籍があって、税金を納めている人なら、等しくサービスを受ける権利があります。逆に測定する側としては、どのような遺伝的な背景を持っているかわからないサンプルに対して、一定のクオリティーを保った検査の成績を返す必要があります。
LSDの各疾患それぞれについても、他の疾患と同様に病的および機能多型の両方を含む遺伝子変異、その頻度および遺伝的背景が先行研究の結果からかなり分かっています。従って、専門家の立場からすると、これまでに分かっている遺伝子変異が人口比率を反映した形で「きちんと見えるのか?」が気になります。
採用例その2(米国ニューヨーク州):遺伝的背景が複雑な場合
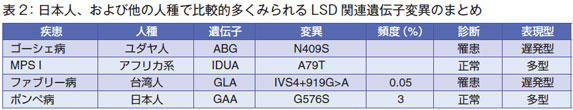
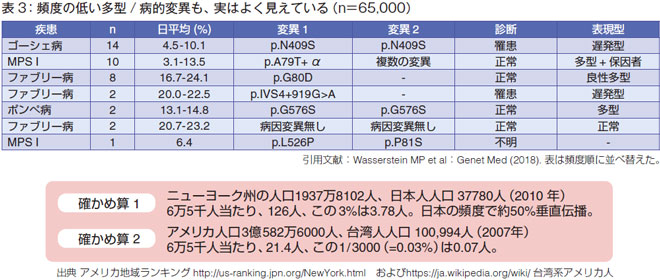
2018年に発表されたWassersteinの論文で、ニューヨーク州の65,000人によるNBSの結果が発表されました(表2、3)。それによると、頻度の低い多型や病的変異も、きちんとよく見えていることが分かりました。
ゴーシェ病のユダヤ人の特徴的な変異N409Sも、一番多く出現しています。MPSⅠ型ではアフリカ系アメリカ人に多い変異も相応な頻度で見えています。それから、台湾で多いファブリー病の遅発型の変異IVS4+919G>Aも2 例で検出されています。ポンペ病は2例で、日本人に多い多型変異G576Sも検出されています。
ゴーシェ病のユダヤ人の特徴的な変異N409Sも、一番多く出現しています。MPSⅠ型ではアフリカ系アメリカ人に多い変異も相応な頻度で見えています。それから、台湾で多いファブリー病の遅発型の変異IVS4+919G>Aも2 例で検出されています。ポンペ病は2例で、日本人に多い多型変異G576Sも検出されています。
確かめ算もあります。ニューヨーク市の人口は1,937万人(2010年)。日本人はニューヨークには3.7 万人ぐらいです。NBS65,000人のうち、日本人は126人です。日本人のポンぺ病のG576S変異の出現頻度は3%ですから、3.78人と予測されます。この論文の結果ではポンペ病のG576S変異は2 例でした。これをどう比べるかですが、50%垂直伝播しているという説明もできるのではないかと推測します。一般的には混血というのは余りないと思うので、数値的にも、結構合っているようです。これがMS/MSのテクノロジーというわけです。
ミズーリ州でDMF 法が採用される1 つの理由
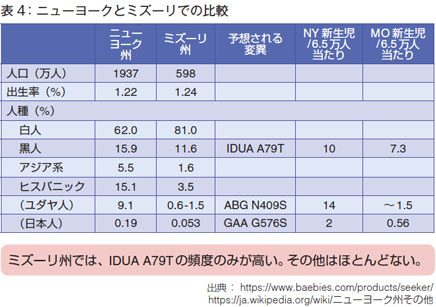 それでは、ニューヨークと異なるミズーリ州の例を紹介します(表4)。これはDigital microfluidics(DMF)法が採用されている州です。ミズーリ州の人口はニューヨークの1/3 で出生率は大体同じです。人種の比率としては黒人がミズーリ州は少なくて、白人が多く、アジア系は少ない。ユダヤ人はニューヨークの1/9位です。
それでは、ニューヨークと異なるミズーリ州の例を紹介します(表4)。これはDigital microfluidics(DMF)法が採用されている州です。ミズーリ州の人口はニューヨークの1/3 で出生率は大体同じです。人種の比率としては黒人がミズーリ州は少なくて、白人が多く、アジア系は少ない。ユダヤ人はニューヨークの1/9位です。新生児65,000 人当たりの検出数で比較すると黒人の割合は7.3人ですから、ニューヨーク10 人と大体同じなんです。しかし、ゴーシェ病の頻度は、ニューヨークでは14 人なのに対し、ミズーリでは1.5 人と1/10になってしまうわけです。
同じアメリカ合衆国連邦の中でも、州によって違うわけです。こういう頻度の違いに対してスクリーニングの方法を検討していくというのは、Population-based screeningにおける費用対効果の検討にも通じ、大切だと考えています。
全体で通してみると、ミズーリ州の場合には、IDUA A79Tの変異以外は頻度が下がるため、そうした場合、MS/MSではなく、蛍光を使うDigital microfluidics(DMF)法で十分であるという話になるわけです。
まとめ
- ライソゾーム病の酵素活性の話についてご紹介させていただきました。
- 酵素活性の測定法の概略をお話しましたが、Population-based screening を自分のところで実施する場合、その集団にどのような遺伝的背景が多いか、予め情報を得てからスクリーニング法を選択することも一案です。
- 好適なスクリーニング法は1 つである理由はありません。いずれにしても最終的には遺伝子検査の実施の数を減らすことが選択基準になるかもしれません。
以上です。